La Hibridación
Para formar compuestos químicos se deben formar enlaces entre los diferentes átomos que forman a la molécula.
|
La Hibridación: sucede cuando se combinan varios orbitales atómicos para formar otros orbitales con la misma energía y mayor estabilidad; las hibridaciones, en el caso de los compuestos orgánicos, son entre el carbono y los átomos que lo rodean, y estos enlaces son los que le van a dar la geometría a la molécula.
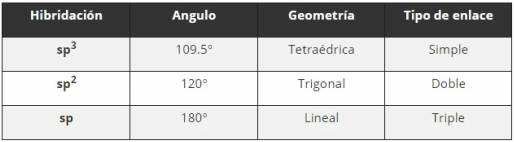
Hibridación sp3Para darle la forma tetraédrica los orbitales de la capa externa (2s, 2px, 2py, 2pz) se mezclan para formar cuatro orbitales híbridos sp3, porque se configuraron un orbital s y tres p.
|
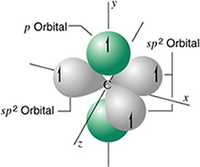
Hibridación sp2Para que esta hibridación ocurra, el carbono debe estar unido a tres átomos, tomemos de ejemplo al eteno CH2=CH2, si tomamos uno de los carbonos éste tiene unido dos hidrógenos y el otro carbono, esta unión forma un triángulo con ángulos de enlace de 120°, a la geometría se le dice trigonal. Se mezclan un orbital s y dos orbitales p, para formar tres orbitales híbridos sp2.
|
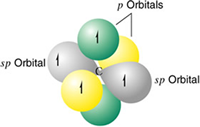
Hibridación sp
|
Aquí el carbono está unido a dos átomos y el ejemplo es el etino o también conocido como acetileno, el ángulo de enlace es de 180° y la geometría es lineal. Se mezclan un orbital s y un orbital p, para formar dos orbitales híbridos sp.
|
HIBRIDACIÓN
|
El orbital molecular es un orbital que explica un enlace covalente que se formó del traslape de dos orbitales atómicos, los cuales tienen un electrón cada uno.
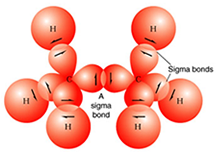
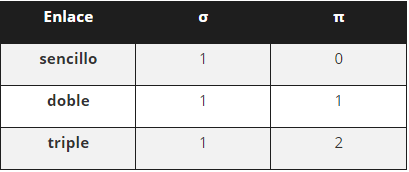
En el caso de la formación del enlace covalente entre dos carbonos se tienen dos tipos de enlaces, el σ y π: enlace sigma (σ) se forma cuando hay superposición de frente de orbitales atómicos; el enlace pi (π) también conocido como simple, se forman cuando hay superposición de orbitales p paralelos.
Los enlaces que forman los distintos elementos que se unen al carbono producen grupos funcionales, que son: